Antecedents i disseny de l'estudi
La retatrutida (LY3437943) és un nou fàrmac monopeptídic que activatres receptors simultàniamentGIP, GLP-1 i glucagó. Per avaluar la seva eficàcia i seguretat en individus amb obesitat però sense diabetis, es va dur a terme un assaig de fase 2, aleatoritzat, doble cec i controlat amb placebo (NCT04881760). Un total de338 participantsamb un IMC ≥30 o ≥27 amb almenys una comorbiditat relacionada amb el pes, van ser assignats aleatòriament per rebre placebo o retatrutida (1 mg, 4 mg amb dos esquemes de titulació, 8 mg amb dos esquemes de titulació o 12 mg) administrat un cop per setmana per injecció subcutània durant 48 setmanes. Elcriteri d'avaluació principalva ser el canvi percentual en el pes corporal a les 24 setmanes, amb criteris d'avaluació secundaris que incloïen el canvi de pes a les 48 setmanes i els llindars de pèrdua de pes categòrics (≥5%, ≥10%, ≥15%).
Resultats clau
-
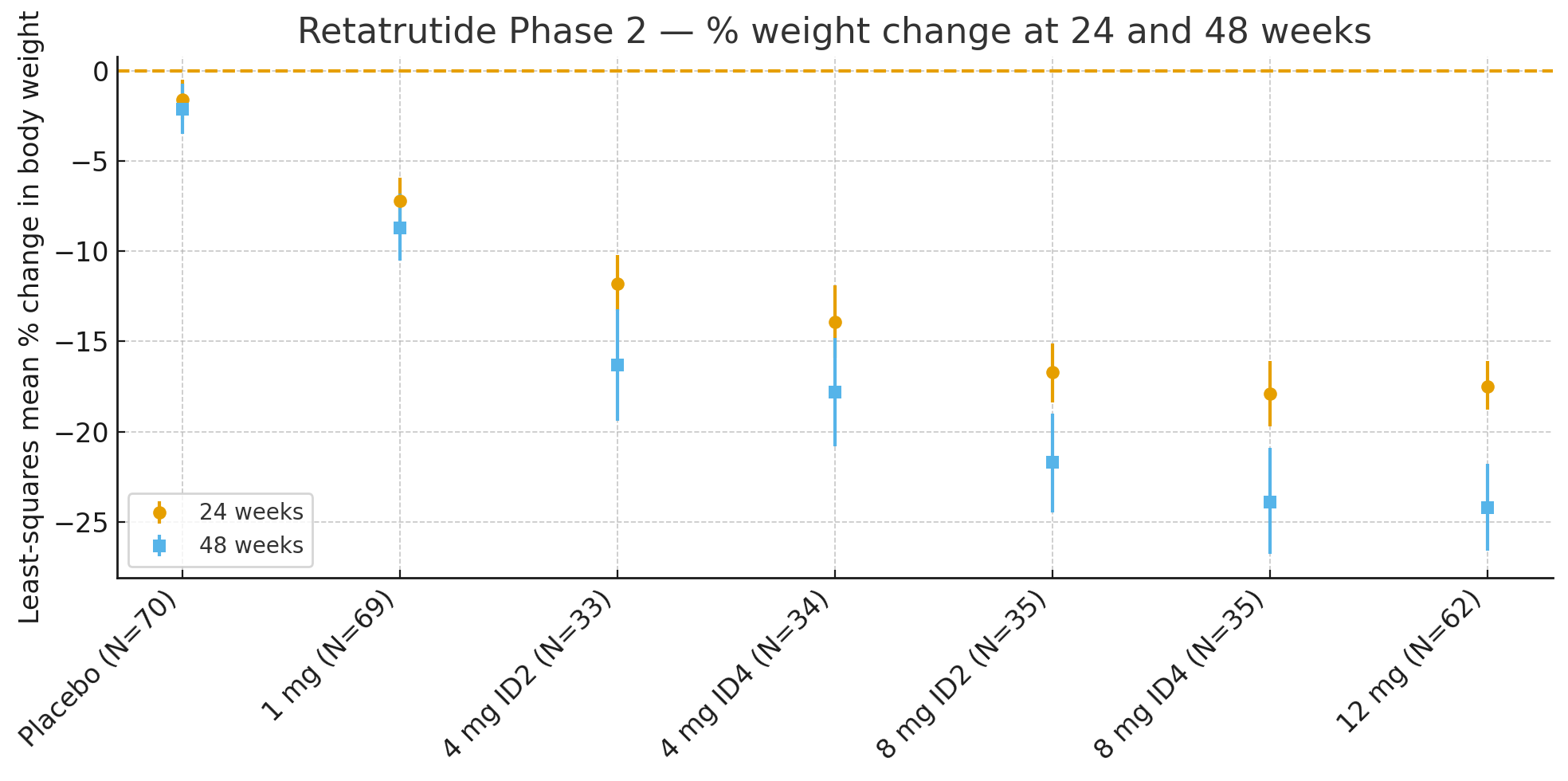
24 setmanes: El canvi percentual mitjà del pes corporal en relació amb el valor basal, calculat per mínims quadrats, va ser
-
Placebo: −1,6%
-
1 mg: −7,2%
-
4 mg (combinats): −12,9%
-
8 mg (combinats): −17,3%
-
12 mg: −17,5%
-
-
48 setmanes: El percentatge de canvi en el pes corporal va ser
-
Placebo: −2,1%
-
1 mg: −8,7%
-
4 mg (combinats): −17,1%
-
8 mg (combinats): −22,8%
-
12 mg: −24,2%
-
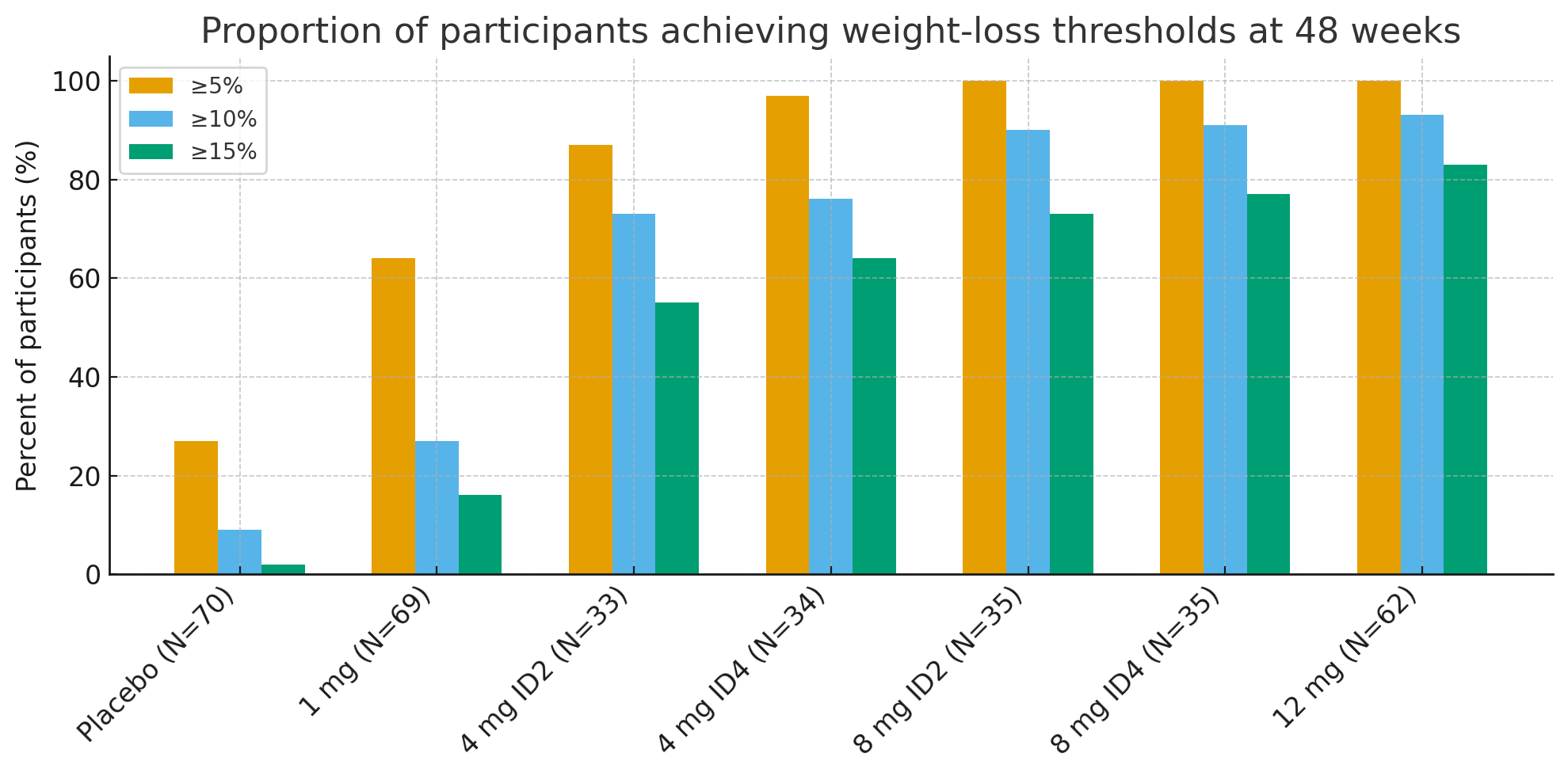
A les 48 setmanes, les proporcions de participants que van assolir llindars de pèrdua de pes clínicament significatius van ser sorprenents:
-
Pèrdua de pes ≥5%: 27% amb placebo vs. 92–100% en grups actius
-
≥10%: 9% amb placebo vs. 73–93% en grups actius
-
≥15%: 2% amb placebo vs. 55–83% en grups actius
En el grup de 12 mg, fins aEl 26% dels participants van perdre ≥30% del seu pes basal, una magnitud de pèrdua de pes comparable a la cirurgia bariàtrica.
Seguretat
Els esdeveniments adversos més comuns van ser gastrointestinals (nàusees, vòmits, diarrea), generalment lleus a moderats i relacionats amb la dosi. Les dosis inicials més baixes (titulació de 2 mg) van reduir aquests esdeveniments. Es van observar augments de la freqüència cardíaca relacionats amb la dosi, que van assolir el màxim a la setmana 24 i després van disminuir. Les taxes de discontinuació van oscil·lar entre el 6 i el 16% entre els grups actius, una mica més altes que les del placebo.
Conclusions
En adults amb obesitat sense diabetis, la retatrutida subcutània setmanal durant 48 setmanes va produirreduccions substancials i dependents de la dosi del pes corporal(fins a un 24% de pèrdua mitjana a la dosi més alta), juntament amb millores en els marcadors cardiometabòlics. Els esdeveniments adversos gastrointestinals van ser freqüents però manejables amb la titulació. Aquestes troballes de la fase 2 suggereixen que la retatrutida podria representar un nou punt de referència terapèutic per a l'obesitat, pendent de confirmació en assajos de fase 3 més grans i a llarg termini.
Data de publicació: 28 de setembre de 2025