Ja el 24 d'agost de 2021, Cara Therapeutics i el seu soci comercial Vifor Pharma van anunciar que el seu primer agonista del receptor opioide kappa difelikeflina (KORSUVA™) havia estat aprovat per la FDA per al tractament de pacients amb malaltia renal crònica (IRC) (pruïja moderada/greu positiva amb tractament d'hemodiàlisi), i que es preveu que es llanci al primer trimestre del 2022. Cara i Vifor van signar un acord de llicència exclusiva per a la comercialització de KORSUVA™ als Estats Units i van acordar vendre KORSUVA™ a Fresenius Medical. Entre elles, Cara i Vifor tenen cadascuna una participació del 60% i el 40% en els ingressos per vendes que no siguin de Fresenius Medical; cadascuna té una participació del 50% en els ingressos per vendes de Fresenius Medical.
La pruïja associada a la IRC (IRC-aP) és una pruïja generalitzada que es produeix amb alta freqüència i intensitat en pacients amb IRC sotmesos a diàlisi. La pruïja es produeix en aproximadament el 60%-70% dels pacients que reben diàlisi, dels quals el 30%-40% tenen pruïja moderada/greu, que afecta greument la qualitat de vida (per exemple, mala qualitat del son) i s'associa amb depressió. No hi ha cap tractament eficaç per a la pruïja relacionada amb la IRC abans, i l'aprovació de Difelikefalina ajuda a abordar l'enorme bretxa de necessitats mèdiques. Aquesta aprovació es basa en dos assajos clínics pivotals de fase III en la sol·licitud de NDA: dades positives dels assajos KALM-1 i KALM-2 als EUA i a nivell mundial, i dades de suport de 32 estudis clínics addicionals, que demostren que KORSUVA™ es tolera bé.
No fa gaire, van arribar bones notícies de l'estudi clínic de la difelikefalina al Japó: el 10-1-2022, Cara va anunciar que els seus socis Maruishi Pharma i Kissey Pharma van confirmar que la injecció de difelikefalina s'utilitza al Japó per al tractament de la pruïja en pacients d'hemodiàlisi. Assajos clínics de fase III Es va complir el criteri d'avaluació principal. 178 pacients van rebre 6 setmanes de difelikefalina o placebo i van participar en un estudi d'extensió obert de 52 setmanes. El criteri d'avaluació principal (canvi en la puntuació de l'escala de valoració numèrica de la pruïja) i el criteri d'avaluació secundari (canvi en la puntuació de la picor a l'escala de gravetat de Shiratori) van millorar significativament respecte al valor inicial en el grup difelikefalina en comparació amb el grup placebo i es van tolerar bé.
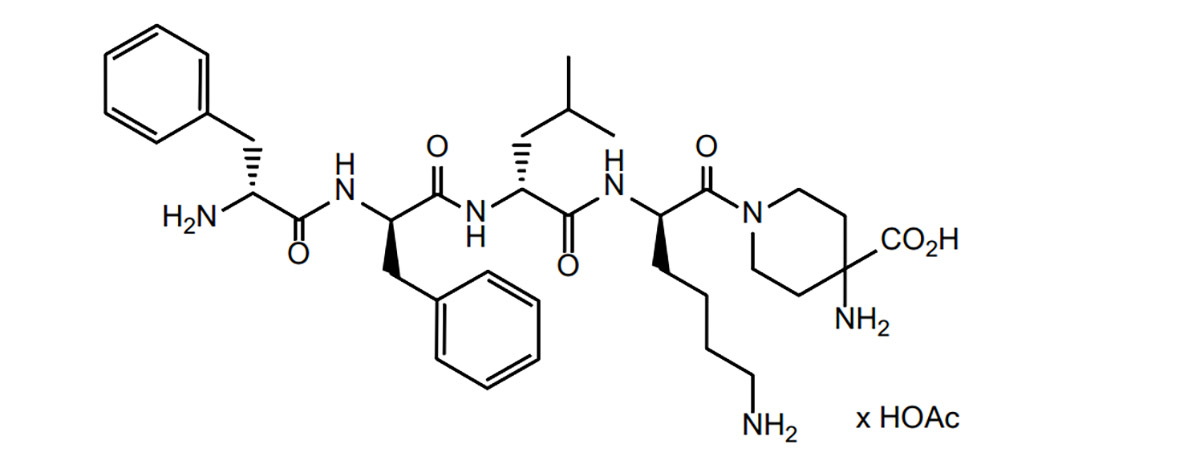
La difelikefalina és una classe de pèptids opioides. A partir d'això, el Peptide Research Institute ha estudiat la literatura sobre pèptids opioides i ha resumit les dificultats i estratègies dels pèptids opioides en el desenvolupament de fàrmacs, així com la situació actual del desenvolupament de fàrmacs.
Data de publicació: 17 de febrer de 2022